先月末に放送された「生きるを伝える」という番組で、全盲のプロドラマーである佐藤尋宣さんのドキュメンタリーが紹介された。子供の頃から目に異常を感じた佐藤さんは、網膜色素変性症と診断されていた。高校生の時にドラムとの運命的出会いが訪れたが、21歳で完全に失明になった。それでも23歳でプロのドラマーになる夢を果たせた。
難病といわれる「網膜色素変性症」という目の病気に明確な効果を示す治療法は確立されていない。その中で、藻類タンパク質を利用した画期的な遺伝子療法の臨床試験が今年(2018年)始まろうとしている。
藻類で本当に目の病気が治すことができるのかと疑問に思う人も多いだろう。今回は、正常な人の視覚と網膜色素変性症の原因、そしてなぜ藻類のタンパク質が人の治療に役立つ事ができるのかを紹介する。
人が物を見る仕組み
そもそも、「物を見る」とは、眼の網膜で受けた光刺激を信号に変えて、網膜神経節細胞という神経細胞を介して情報が脳へと送られ、大脳皮質の視覚野で形や色、明るさ、動き、位置などが分析されることを意味する。神経細胞の細胞内の素早い伝播には、細胞内外の「膜電位」の差を利用した電気信号が用いられている。
網膜についてもう少し詳しく見ていくことにする。眼球の内側、一番奥にある網膜という薄い膜状の部分には光や色を感じるのに重要な視細胞(桿体細胞と錐体細胞)がたくさん存在している。桿体細胞は高感度で弱い光を感じ取る細胞であり、眼球1つに1億個以上も存在し、中心窩を除く網膜全体に分布している。一方、錐体細胞は強い光と色を検知する細胞であり、網膜の中心部である黄斑部に600万個ほど高密度に存在している。
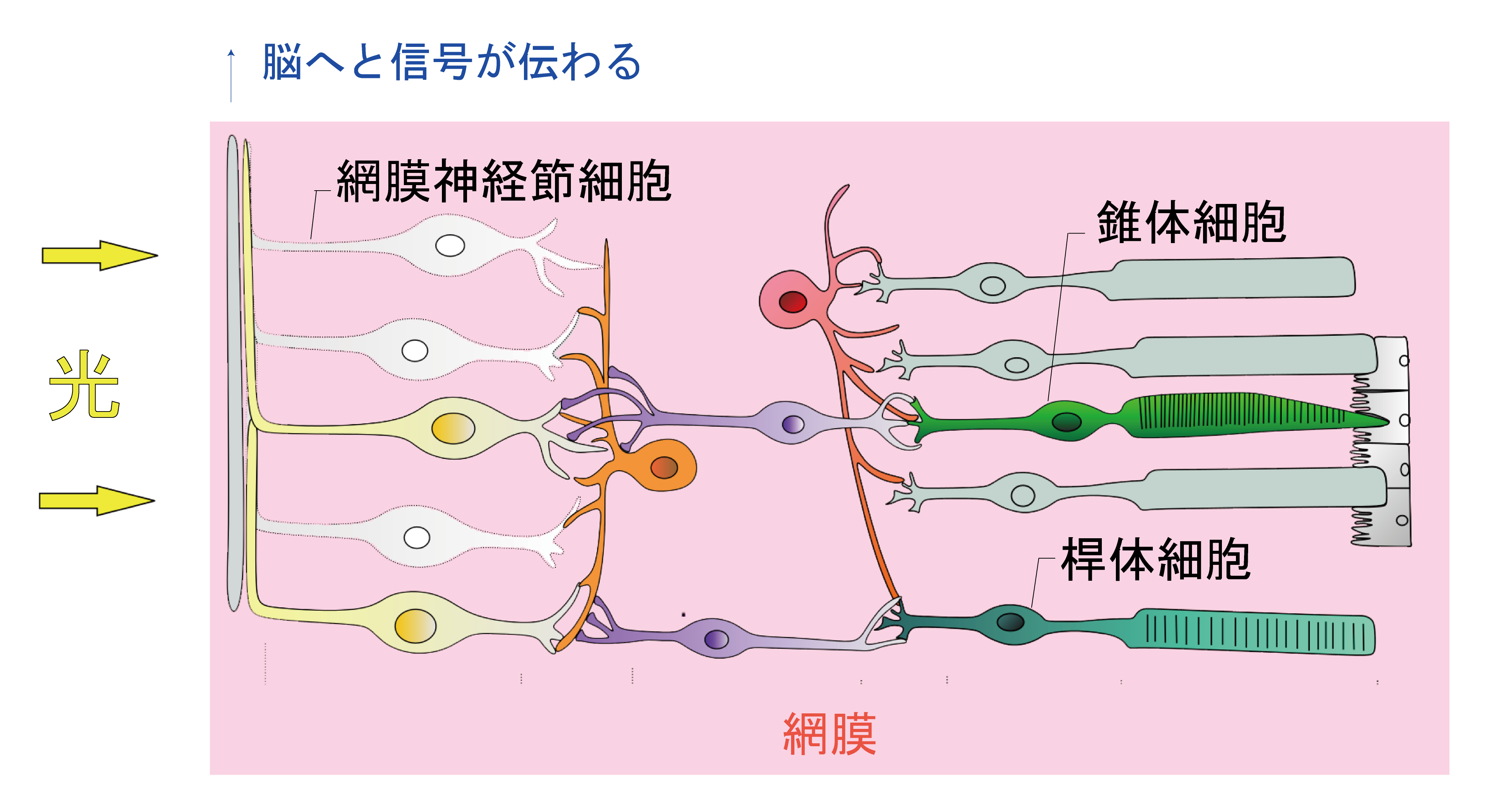
網膜の構造/”Retina“よりModia編集部が作成
網膜色素変性症とはどんな病気だろう?
網膜色素変性症は遺伝要因が大きいとされ、3000~4000人に1人の割合で発症する難病であり、世界で約150万人の人が罹患していると推定されている。網膜色素変性症は先進国における遺伝性失明症の主因であり、日本では、緑内障、糖尿病網膜症に続き、中途失明の原因となっている。病原となる遺伝子変異は60種類以上が同定されているものの、常染色体優性遺伝、常染色体劣性遺伝、X連鎖劣性遺伝と様々な遺伝形式によるため、治療において原因遺伝子の特定が困難である。
網膜色素変性症という疾患は、初期段階では桿体細胞の機能が失われ、夜盲症や視野狭窄が現れる。錐体細胞の機能は網膜色素変性症に関連する遺伝子の変異には影響されないが、発症すると徐々に色覚異常や中心視力の低下が進行し、最終的には失明に至る。現時点で、臨床的に明確な効果を示す治療法は確立されておらず、世界中で様々な治療法の研究が行われている。
藻類の光受容性タンパク質の本来の機能
藻類は光合成をして生きているため、光は必要不可欠である。光合成を効率よく行うため、多くの藻類は鞭毛を動かして最適な光環境へと自ら移動できる運動機構をもつ。眼点という部位で光の方向性や強さを感知して、弱光下では光に寄ってくる正の走行性を、強光下では光を回避するため負の走行性を示す。眼点には光受容性タンパク質が存在している。
藻類の中でモデル生物といわれている緑藻綱クラミドモナス(Chlamydomonas reinhardii)では、光受容性タンパク質の研究が進んでいる。クラミドモナスの光感受性タンパク質のうち、チャネルロドプシンⅡ(ChR2)は、光を感じると陽イオン(Na+やCa2+)を細胞外から細胞内に流入する光受容イオンチャネルである。チャネルロドプシンⅡはタンパク質分子単独で光を感受すると膜電位を変化させることができる。クラミドモナスは光を受容すると、眼点のチャネルロドプシンが膜電位差を生じさせ、それが鞭毛に伝わり、鞭毛を動かして目的の方向へと細胞が進んでいく。
藻類の光感受性タンパク質の治療への応用
藻類タンパク質を利用した治療法の臨床試験を行う企業は、フランスを拠点とする、2013年に創立されたGenSight Biologics社というバイオファーマである。同社は既にヒトの遺伝子を用いた様々な網膜神経変性疾患や中枢神経系疾患の新規治療法の開発を進めている(詳細は末章「希少疾病用医薬品の開発に期待」に記載)。
今年1月、GenSight Biologics社は、藻類光受容性タンパク質による網膜色素変性症 (retinitis pigmentosa) への遺伝子治療の第I相/第II相臨床試験開始の申請がイギリスの医薬品・医療製品規制庁に承認されたことを発表した。試験は2018年の第1四半期に開始される予定である。
同社の開発する治療法は、クラミドモナス(Chlamydomonas noctigama)の持つチャネルロドプシンを改変した光受容イオンチャネルを人の網膜神経節細胞に導入し発現させることで、本来は光受容をしない網膜神経節細胞に、光受容機能と膜電位差を同時に生じさせる試みである。桿体細胞で光を受容できなくても、その先に続く網膜神経節細胞で光を受容できるので、光感知能及び視覚を回復させることが大いに期待されている。
最近注目を集める、オプトジェネティクスとは?
光(opto)と遺伝学(genetics)を組み合わせたオプトジェネティクス(光遺伝学、optogenetics)と呼ばれる技術が、近年非常に注目を浴びている。世界的に権威のある学術誌”Nature”の姉妹誌、”Nature Methods”が発表する「Method of the year 2010」にも選ばれ、ノーベル賞に一番近い画期的な技術の一つである。以下のビデオでも紹介されているが、クラミドモナスのチャネルロドプシンの神経細胞への導入は、比較的短い遺伝子配列の導入で済む点、タンパク質発現後の修飾が不要である点、そして神経伝播並みの素早い膜電位を光刺激と同期して発生することができる点で、光刺激技術の中で最も実用的な方法といわれている(石塚&八尾, 2008)。GenSight Biologics社の網膜色素変性に対する藻類光受容性タンパク質の導入の遺伝子療法もオプトジェネティクス技術に当たる。
Method of the Year 2010: Optogenetics – by Nature Video
This video shows how scientists can control the behaviour of cells simply by switching on a light. The technique, known as optogenetics, is teaching us about everything from how we wake up to how we learn. That’s why Nature Methods has named optogenetics as its Method of the Year 2010.
現在、オプトジェネティクス技術に基づく遺伝子療法の開発では複数のベンチャー企業が行っている。例えば、2016年2月にはアステラス製薬社とクリノ社が連携し、網膜色素変性症における遺伝子治療薬の開発・商業化ライセンス契約の締結を発表した。また、窪田製薬ホールディングスは2016年4月に英国マンチェスター大学と、網膜色素変性を含む網膜変性疾患の治療を対象とするヒトロドプシンによるオプトジェネティクス治療の開発権、並びに全世界での販売権を得る独占契約を締結した。
希少疾病用医薬品の開発に期待
GenSight Biologics社が先行して開発している遺伝子治療薬GS010は、ミトコンドリアDNAの変異によるレーベル遺伝性視神経症(Laber’shereditary optic neuropathy)の治療薬として、単回投与により持続的な視力改善効果が発表されている。今年2月に第I / II相臨床試験および2年間の長期追跡調査試験が終了し、現在は、第III相臨床試験が米国と欧州で検証されている。
これまで医療・製薬業界では患者数の比較的多い疾患を中心に治療開発が優先されてきた。一方、患者数が少なく、診断法や治療法の確立していない希少疾患においては、市場が小さいため、疾患の解明や治療法の開発が非常に困難な環境にあり、未だ十分な研究が行われていない。こうした中、希少疾病用医薬品の開発を促進するために、世界各国でも様々な制度や優遇措置が策定されるようになっており、今後開発が進展することを期待したい。
難病と闘う患者、そして彼らを支えている周りの人達の世界を想像するだけでも辛い。難病が”治る病気”に変わる日が一日でも早く訪れることを願っている。大きなことができるわけでもないが、希少疾病用医薬品の開発を積極的に行う製薬企業に対しては、個人的に応援していきたい。
参考資料
・Vaidya P, Vaidya A. Retinitis Pigmentosa: Disease Encumbrance in the Eurozone. Int J Ophthalmol Clin Res. 2:030 (2015)
・Awasthi, M., Ranjan, P., Sharma, K., Veetil, S. K., & Kateriya, S. (2016). The trafficking of bacterial type rhodopsins into the Chlamydomonas eyespot and flagella is IFT mediated. Scientific reports, 6, 34646.
・Wakabayashi, K. I., Misawa, Y., Mochiji, S., & Kamiya, R. (2011). Reduction-oxidation poise regulates the sign of phototaxis in Chlamydomonas reinhardtii. Proceedings of the National Academy of Sciences, 108(27), 11280-11284.
・石塚徹, & 八尾寛. (2008). 光受容イオンチャネル・チャネルロドプシン 2 を用いたニューロンの光刺激. 生物物理, 48(3), 180-184.
・http://www.newsweek.com/medical-breakthrough-help-blind-see-using-genes-algae-782716
・http://www.nanbyou.or.jp/entry/4660
・http://news.algaeworld.org/2018/01/breakthrough-in-restoring-vision-genes-from-algae-could-cure-blindness/
・https://www.gensight-biologics.com/2018/02/20/gensight-biologics-announces-publication-of-positive-data-from-phase-i-ii-trial-and-long-term-follow-up-of-gs010-in-ophthalmology-the-journal-of-the-american-academy-of-ophthalmology/
・https://patents.google.com/patent/WO2017187272A1/en
・https://ghr.nlm.nih.gov/condition/retinitis-pigmentosa
・http://kabutoyohou.com/2016/04/05/405309/
参考画像
”Retina“© 2005 Pancrat/CC BY 3.0









_e2-300x300.png)



SHARE